貧血
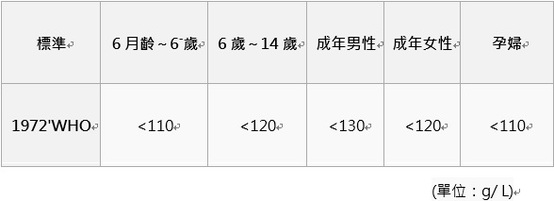
貧血是臨床最常見的表現之一,然而它不是一種獨立疾病,可能是一種基礎的或有時是較複雜疾病的重要臨床表現,一旦發現貧血,必須查明其發生原因。在一定容積的循環血液內紅血球計數、血紅蛋白量以及紅細胞壓積均低於正常標準者稱為貧血。其中以血紅蛋白最為重要,成年男性低於120g/L(12.0g/dl),成年女性低於110 g/L (11.0/dl) ,一般可認為貧血。在一定容積的循環血液內紅血球計數、血紅蛋白量以及紅細胞壓積均低於正常標準者稱為貧血。因紅血球容量測定複雜,臨床常以血紅蛋白濃度(Hb)、紅血球計數(RBC)、血球壓積(Hct)等指標替代,這就可能造成:
診斷
以血紅蛋白濃度(Hb)為依據,適用於海平面居民:
貧血是臨床最常見的表現之一,然而它不是一種獨立疾病,可能是一種基礎的或有時是較複雜疾病的重要臨床表現,一旦發現貧血,必須查明其發生原因。在一定容積的循環血液內紅血球計數、血紅蛋白量以及紅細胞壓積均低於正常標準者稱為貧血。其中以血紅蛋白最為重要,成年男性低於120g/L(12.0g/dl),成年女性低於110 g/L (11.0/dl) ,一般可認為貧血。在一定容積的循環血液內紅血球計數、血紅蛋白量以及紅細胞壓積均低於正常標準者稱為貧血。因紅血球容量測定複雜,臨床常以血紅蛋白濃度(Hb)、紅血球計數(RBC)、血球壓積(Hct)等指標替代,這就可能造成:
- 假性貧血:紅血球容量正常,但血容量增加導致血液稀釋,使Hb、RBC、Hct等濃度指標下降。見於妊娠、充血性心力衰竭、脾大、低白蛋白血症、巨球蛋白血症等。
- 漏診貧血:貧血伴血液濃縮時,Hb、RBC、Hct等濃度指標下降不及紅血球容量,可能導致漏診。見於急性失血性貧血早期等。
診斷
以血紅蛋白濃度(Hb)為依據,適用於海平面居民:
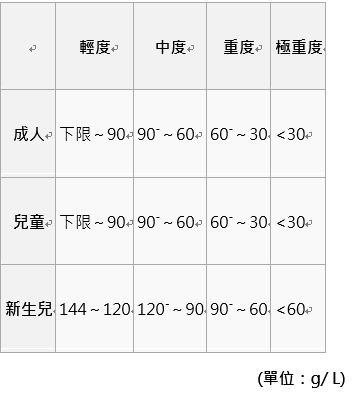
分級
依據血紅蛋白濃度(Hb)分級
依據血紅蛋白濃度(Hb)分級
類型
(2) 正細胞性貧血:MCV在80fL~100fL。
(3)小細胞性貧血:MCV<80fL。
(2)造血細胞異常所致貧血
(3)造血調控異常所致貧血
2. 紅血球破壞過多性貧血:即溶血性貧血
3. 失血性貧血
病因及發病機制
紅血球生成減少性貧血
形成。
(2) B細胞功能亢進,經抗骨髓細胞抗體介導:見於免疫相關性全血細胞減少。
2. 骨髓基質細胞及造血微環境異常:見於骨髓炎、骨髓壞死、骨髓纖維化、骨髓硬化症、大理石病、髓外腫瘤骨髓
轉移等。
3. 造血調節因子水平異常:見於慢性病性貧血。其機制可細分為:
(1) 正性造血調節因子水平低下:腎功能不全、慢性肝病、垂體功能低下、甲狀腺功能減退均可導致EPO生成不
足。
① 腎衰,特別是雙腎切除後,體內只剩下腎外(主要是肝臟)來源的EPO,因此EPO水平降至正常的10%。低下的
EPO水平必然導致紅系造血能力下降,因此,慢性腎衰,特別是雙腎切除後的患者,如果沒有輸血或補充外源
EPO的話,往往有嚴重的貧血,血紅蛋白濃度常在50g/L以下。
② 罕見的情況下,機體產生抗EPO抗體,此時血流中的EPO水平往往低至無法檢測,可導致嚴重的純紅細胞再生
障礙性貧血。
③ 慢性感染、炎症性疾病、腫瘤可導致IL-1、IL-6、TNFα等炎症因子釋放,可抑制EPO的合成。
(2) 負性造血調節因子水平升高:慢性感染、炎症性疾病、腫瘤可導致TNF、IFN等負性造血調節因子釋放,抑製造
血。
紅細胞破壞過多性貧血(即溶血性貧血)
(1) 先天性紅細胞卟啉代謝異常:紅細胞生成性血卟啉病。
(2) 繼發性紅細胞卟啉代謝異常:鉛中毒。
2. 珠蛋白異常所致溶血
(1) 珠蛋白肽鏈合成量的異常所致溶血:海洋性貧血。
(2) 珠蛋白肽鏈的結構異常所致溶血:異常血紅蛋白病。
3. 遺傳性紅細胞酶缺乏所致溶血:如G6PD缺乏、丙酮酸激酶缺乏等。
4. 紅細胞膜異常所致溶血
(1) 遺傳性紅細胞膜缺陷:如遺傳性棘形細胞增多症、遺傳性口形細胞增多症、遺傳性橢圓細胞增多症、遺傳
性球形細胞增多症。
(2) 獲得性血細胞膜GPI錨連蛋白異常:陣發性睡眠性血紅蛋白尿。
紅細胞胞外環境異常所致溶血
1. 免疫性溶血
(1)自身免疫性溶血
(2)同種免疫性溶血:血型不符所致的急性輸血相關性溶血或慢性輸血相關性溶血,新生兒溶血症。
2. 血管性溶血
(1)微血管病性溶血:彌散性血管內凝血、血栓性血小板減少性紫癜、溶血尿毒症候群。
(2)血管壁反覆擠壓:行軍性血紅蛋白尿。
(3)血管壁異常:血管炎、瓣膜病、人工瓣膜植入術後。
3. 物理因素:滲透壓改變。
4. 化學因素:氧化劑所致獲得性高鐵血紅蛋白血症。
5. 生物因素:瘧疾、黑熱病、蛇毒
失血性貧血
症状
貧血症状的有無或輕重,取決於貧血的程度、貧血發生的速度、循環血量有無改變、病人的年齡以及心血管系統的代償能力等。貧血發生緩慢,機體能逐漸適應,即使貧血較重,尚可維持生理功能;反之,如短期內發生貧血,即使貧血程度不重,也可出現明顯症状。年老體弱或心、肺功能減退者,症状較明顯。
貧血的一般症状,體征如下:
常見貧血症狀
- 依貧血發展速度分:急性貧血、慢性貧血。
- 依紅血球形態分:主要參考平均紅細胞體積(MCV)
(2) 正細胞性貧血:MCV在80fL~100fL。
(3)小細胞性貧血:MCV<80fL。
- 依骨髓紅系增生情況分:
- 增生性貧血
- 增生不良性貧血
- 依病因、發病機制分:
- 紅血球生成減少性貧血
(2)造血細胞異常所致貧血
(3)造血調控異常所致貧血
2. 紅血球破壞過多性貧血:即溶血性貧血
3. 失血性貧血
病因及發病機制
紅血球生成減少性貧血
- 造血原料異常所致貧血
- 缺鐵性貧血:鐵來源不足、吸收障礙、轉運障礙、利用障礙、丟失過多。
- 鐵粒幼細胞性貧血:多種原因導致的紅細胞鐵利用障礙。
- 巨幼細胞貧血:葉酸和/或維生素B12來源不足、吸收障礙、轉運障礙、利用障礙。
- 造血細胞異常所致貧血
- 純紅細胞再生障礙性貧血:骨髓紅系造血干祖細胞異常。
- 先天性紅細胞生成異常性貧血:遺傳性紅系造血干祖細胞良性克隆異常導致紅系無效造血。
- 造血系統惡性克隆性疾病:多能造血幹細胞或髓系干祖細胞異常干擾正常紅系造血,如骨髓增生異常症候群、白血病等。
- 繼發性骨髓抑制:見於苯、抗癌化療藥、氯霉素、金鹽、電離輻射、病毒感染(如EBV、HIV、肝炎病毒、登革病毒)。
- 造血調節異常所致貧血
- 針對造血細胞的自身免疫:
形成。
(2) B細胞功能亢進,經抗骨髓細胞抗體介導:見於免疫相關性全血細胞減少。
2. 骨髓基質細胞及造血微環境異常:見於骨髓炎、骨髓壞死、骨髓纖維化、骨髓硬化症、大理石病、髓外腫瘤骨髓
轉移等。
3. 造血調節因子水平異常:見於慢性病性貧血。其機制可細分為:
(1) 正性造血調節因子水平低下:腎功能不全、慢性肝病、垂體功能低下、甲狀腺功能減退均可導致EPO生成不
足。
① 腎衰,特別是雙腎切除後,體內只剩下腎外(主要是肝臟)來源的EPO,因此EPO水平降至正常的10%。低下的
EPO水平必然導致紅系造血能力下降,因此,慢性腎衰,特別是雙腎切除後的患者,如果沒有輸血或補充外源
EPO的話,往往有嚴重的貧血,血紅蛋白濃度常在50g/L以下。
② 罕見的情況下,機體產生抗EPO抗體,此時血流中的EPO水平往往低至無法檢測,可導致嚴重的純紅細胞再生
障礙性貧血。
③ 慢性感染、炎症性疾病、腫瘤可導致IL-1、IL-6、TNFα等炎症因子釋放,可抑制EPO的合成。
(2) 負性造血調節因子水平升高:慢性感染、炎症性疾病、腫瘤可導致TNF、IFN等負性造血調節因子釋放,抑製造
血。
紅細胞破壞過多性貧血(即溶血性貧血)
- 紅細胞異常所致溶血
(1) 先天性紅細胞卟啉代謝異常:紅細胞生成性血卟啉病。
(2) 繼發性紅細胞卟啉代謝異常:鉛中毒。
2. 珠蛋白異常所致溶血
(1) 珠蛋白肽鏈合成量的異常所致溶血:海洋性貧血。
(2) 珠蛋白肽鏈的結構異常所致溶血:異常血紅蛋白病。
3. 遺傳性紅細胞酶缺乏所致溶血:如G6PD缺乏、丙酮酸激酶缺乏等。
4. 紅細胞膜異常所致溶血
(1) 遺傳性紅細胞膜缺陷:如遺傳性棘形細胞增多症、遺傳性口形細胞增多症、遺傳性橢圓細胞增多症、遺傳
性球形細胞增多症。
(2) 獲得性血細胞膜GPI錨連蛋白異常:陣發性睡眠性血紅蛋白尿。
紅細胞胞外環境異常所致溶血
1. 免疫性溶血
(1)自身免疫性溶血
(2)同種免疫性溶血:血型不符所致的急性輸血相關性溶血或慢性輸血相關性溶血,新生兒溶血症。
2. 血管性溶血
(1)微血管病性溶血:彌散性血管內凝血、血栓性血小板減少性紫癜、溶血尿毒症候群。
(2)血管壁反覆擠壓:行軍性血紅蛋白尿。
(3)血管壁異常:血管炎、瓣膜病、人工瓣膜植入術後。
3. 物理因素:滲透壓改變。
4. 化學因素:氧化劑所致獲得性高鐵血紅蛋白血症。
5. 生物因素:瘧疾、黑熱病、蛇毒
失血性貧血
- 急性失血性貧血
- 慢性失血性貧血
症状
貧血症状的有無或輕重,取決於貧血的程度、貧血發生的速度、循環血量有無改變、病人的年齡以及心血管系統的代償能力等。貧血發生緩慢,機體能逐漸適應,即使貧血較重,尚可維持生理功能;反之,如短期內發生貧血,即使貧血程度不重,也可出現明顯症状。年老體弱或心、肺功能減退者,症状較明顯。
貧血的一般症状,體征如下:
- 軟弱無力:疲乏、睏倦,是因肌肉缺氧所致。為最常見和最早出現的症状。
- 皮膚、粘膜蒼白:皮膚、粘膜、結膜以及皮膚毛細血管的分布和舒縮狀態等因素的影響。一般認為瞼結合膜、手掌大小魚際及甲床的顏色比較可靠。
- 心血管系統:心悸為最突出的症状之一,有心動過速,在心尖或肺動脈瓣區可聽到柔和的收縮期雜音,稱為貧血性雜音,嚴重貧血可聽到舒張期雜音。嚴重貧血或原有冠心病,可引起心絞痛、心臟擴大、心力衰竭。
- 呼吸系統::氣急或呼吸困難,大都是由於呼吸中樞低氧或高碳酸血症所致。
- 中樞神經系統:頭暈、頭痛、耳鳴、眼花、注意力不集中、嗜睡等均為常見症状。暈厥甚至神志模糊可出現於貧血嚴重或發生急驟者,特別是老年患者。
- 消化系統:食慾減退、腹脹、噁心、便秘等為最多見的症状。
- 生殖系統:婦女患者中常有月經失調,如閉經或月經過多。在男女兩性中性慾減退均多見。
- 泌尿系統:貧血嚴重者可有輕度蛋白尿及尿濃縮功能減低。
常見貧血症狀
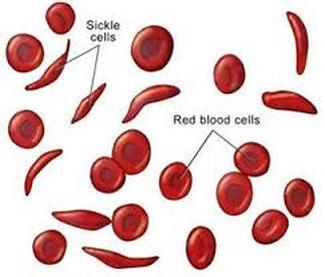
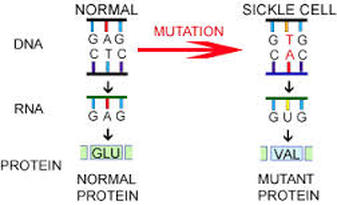
- 鐮型血球貧血症(Sickle Cell Anemia)
正常血红素的蛋白質構造呈球形,而突變後的結構發生改變,在氧氣不足的情況下,例如登高山或劇烈運動時,易凝聚成長條狀結構使紅血球扭曲成鐮刀型。這個結果除了會導致紅血球的攜氧量降低之外,同時也會傷害紅血球的細胞膜,並使血液的黏滯度增大;且鐮刀型紅血球較硬,不容易變形,易造成微血管阻塞,干擾血流的順暢,使得部分組織不易獲得氧氣,而導致局部缺血和梗塞。鐮型血球貧血症患者容易併發感染沙門桿菌(Salmonella spp.),或是産生脾腫大、胸腹疼痛等現象。通常健康的紅血球的壽命約為120日,但鐮刀形紅血球壽命卻沒有這麼長,有些只有10至20日。,加上血紅蛋白纖維長鏈會傷害細胞膜,使紅血球發生溶血(haemolysis),導致嚴重貧血(anaemia)。由於鐮型血球的等位基因發生突變,會影響到許多性狀,因此稱之為基因多效應 (Pleiotropy)。
就自然法則而言,突變是隨機沒有目的性的。瘧疾在非洲造成許多死亡,然而鐮型血球貧血症患者因血球的型態與正常人不同,紅血球很容易破裂而溶血,且血紅蛋白聚合成的纖維長鏈令到瘧原蟲不能消化血紅蛋白,瘧原蟲無法在鐮刀形紅血球內成長,因禍得福而不會感染瘧疾。由於此貧血症患者大量存活並生育下一代,使得此突變基因序列成功地傳遞給子代,故鐮刀型貧血症在黑種人身上的發生率約為六百分之一,這在其他人種相當罕見。
就自然法則而言,突變是隨機沒有目的性的。瘧疾在非洲造成許多死亡,然而鐮型血球貧血症患者因血球的型態與正常人不同,紅血球很容易破裂而溶血,且血紅蛋白聚合成的纖維長鏈令到瘧原蟲不能消化血紅蛋白,瘧原蟲無法在鐮刀形紅血球內成長,因禍得福而不會感染瘧疾。由於此貧血症患者大量存活並生育下一代,使得此突變基因序列成功地傳遞給子代,故鐮刀型貧血症在黑種人身上的發生率約為六百分之一,這在其他人種相當罕見。
- 地中海貧血(Thalassemia)
種類
根據血紅蛋白中不同位置的損害可分成兩類:α地中海貧血與β地中海貧血。α地中海貧血是血紅蛋白中的α血紅蛋白鏈有缺損,β地中海貧血則是血紅蛋白中的β血紅蛋白鏈有缺損。鐮刀型紅血球疾病,又名鐮刀型貧血(Sickle Cell Anemia)和地中海貧血不同的是它只發生β血紅蛋白的缺陷。
1. α地中海貧血
α地中海貧血的患者會在HBA1、HBA2這兩個基因發生異常。在成人造成β蛋白鏈過度製造,在新生兒則是γ蛋白鏈過多。過多的β蛋白鏈形成四聚物(tetramers)使紅血球的攜氧能力降低。
2. β地中海貧血
β地中海貧血的患者則是在第11號染色體上的HBB基因發生突變。不正常的細胞會製造過量的α蛋白鏈,然後結合在紅血球的細胞膜上造成細胞膜損壞;若其濃度過高,則有形成有毒聚集體(aggregates)的可能。
症狀
地中海貧血症有隱性、輕型和重型之分。重型患者需要終生定期的輸血和接受藥物治療;而兩個隱性或輕度患者結婚,他們的下一代則有1/4機會患有重度地中海貧血症。相反地,兩者中只有一位是存有地中海貧血症基因的話,不論程度如何,則下一代沒有此問題或只帶有隱性或輕度。
由於地中海型貧血的患者缺少正常的血紅素,紅血球攜氧功能差,體內主要造血器官骨髓與次要造血器官肝臟、脾臟均會進行旺盛的造血作用,但造出的紅血球也多半品質不佳,容易被破壞,成為惡性循環。骨髓增生會侵犯周圍的皮質骨,使骨骼較脆弱。旺盛的造血作用會消耗極多的養分與能量,使身體其他部位的養分供需失調。不斷的輸血可以改善貧血的症狀,也可避免過度的造血作用,但血紅素中的鐵質會過度存在身體中,並堆積至各重要器官造成器官病變。
而生活中,地中海貧血患者因血紅素帶氧量不足而影響患者在體力上的差異,患者不適宜進行太激烈的運動,還需要打除鐵針去除體內多餘的鐵質。另外亦因為血紅素不足的關係,患者比較容易有頭暈、頭痛甚至腰痛的症狀。