抗體(antibody)
抗體指機體的免疫系統在抗原刺激下,由B 淋巴細胞或記憶細胞增殖分化成的漿 細胞所產生的、可與相應抗原發生特異性結合的免疫球蛋白。主要分佈在血清中,也分佈於組織液及外分泌液中。
概念
最初有人用電泳證明血清中抗體活性在γ球蛋白部分,故曾把抗體統稱為丙種(γ)球蛋白。後來發現,抗體並不都在γ區;並且位於γ區的球蛋白,也不一定都具有抗體活性。
1964年,世界衛生組織舉行專門會議,將具有抗體活性以及與抗體相關的球蛋白統稱為免疫球蛋白(Ig),如骨髓瘤蛋白,巨球蛋白血症、冷球蛋白血症等患者血清中存在的異常免疫球蛋白以及正常人天然存在的免疫球蛋白亞單位等。因而免疫球蛋白是結構化學的概念,而抗體是生物學功能的概念。可以說,所有抗體都是免疫球蛋白,但並非所有免疫球蛋白都是抗體。
結構
抗體是一種高分子球狀血液蛋白質,重量約為150kDa。由於在部分胺基酸殘基中含有糖鏈,抗體也是一種糖蛋白。能發揮功能的基本單位是一個免疫球蛋白單體。在分泌形態的抗體中包括:二聚體IgA、真骨附類魚的四聚體IgM以及哺乳動物的五聚體IgM。
可發生變化的部分稱為V區(或變化區、可變區),而不變的部分稱為C區(或恆定區)。
免疫球蛋白結構域
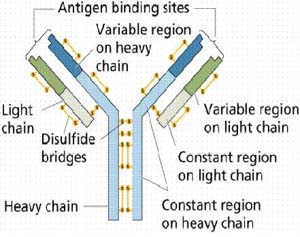
抗體的單體是一個Y形的分子,有4條多肽鏈組成。其中包括兩條相同的重鏈,以及兩條相同的輕鏈,之間由雙硫鍵連接在一起[16]。每一條鏈均由稱為免疫球蛋白結構域的多個結構域所組成。每一個結構域大約包含70至110個胺基酸,並根據大小和功能分門別類。例如可變域IgV以及恆定域IgC)[20]。它們的摺疊方式很特別:通過兩次β摺疊將另一條鏈捲入其中形成三明治狀,互相之間通過半胱氨酸和其它帶電荷胺基酸緊密結合。
重鏈
哺乳動物的免疫球蛋白重鏈有5種,分別用希臘字母記為:α、δ、ε、γ以及μ。根據重鏈類型的不同,抗體被分為不同的種型,它們被發現依序分別存在於抗體IgA、IgD、IgE、IgG以及IgM中。不同的重鏈其大小和組成各不相同:α和γ大約有450個胺基酸組成,而μ和ε大約有550個胺基酸組成。
每一條重鏈有兩個區域:恆定區與可變區。同種型的抗體,其恆定區都是一樣的,但不同種型之間該區域是不相同的。例如:γ、α以及δ型重鏈由三個免疫球蛋白結構域串聯而成,並且還有一個用於增加彈性的鉸鏈區;而μ及ε型重鏈則包括四個免疫球蛋白結構域。不同B細胞所生產抗體的重鏈可變區是不同的,但是同一個B細胞及其克隆體所生產的不同種型抗體的可變區則是完全相同的。重鏈的可變區由一個結構域組成,包含大110個胺基酸。
輕鏈
免疫球蛋白輕鏈由大約211至217個胺基酸組成,分為兩個結構域,分別是恆定區和可變區。哺乳動物的輕鏈有兩種,分別命名為λ(lambda)和κ(kappa)。每一個抗體的兩個輕鏈永遠是完全相同的,例如對於哺乳動物而言,同一個抗體要麼是λ型,要麼是κ,不會同時存在。在如軟骨魚綱(鯊魚)及真骨下綱的低級脊椎動物中,還可發現其它類型的輕鏈,如ι(iota)型。
CDRs、Fv、Fab以及Fc結構域
抗體的某些部分具有獨特的功能。比如說Y形的臂區,包含了兩個可以結合抗原的點位,是識別外來物的關鍵所在。該區域被稱為Fab區,即抗原結合區段(fragment, antigen binding)。無論是重鏈還是輕鏈,抗原結合區段均包括一個可變區與一個恆定區,其中可變區的互補位成型於抗體單體胺基酸鏈的末端。可變區又被稱為FV區,是與抗體結合的最關鍵區域,無論是輕鏈還是重鏈都包含該區域。實際上可變區的變化並非隨機或者均勻散布的。更具體的說,這些變化分布在三個可變的β摺疊-轉角上,該區域被稱為互補決定區(Complementarity Determining Region,CDR),也叫做高變區。喬西亞(Chothia)等人,以及後來的諾斯等人對互補決定區的結構進行了歸類。在免疫網路理論*中,每個抗體的互補決定區又被稱為獨特型或者基因型。適應性免疫系統的適應過程,就是依靠有各個獨特型之間的互動來進行調整的。
Y形結構的基座的作用是調節免疫細胞的活動,該區域被稱為Fc區(Fragment crystallizable region,可結晶區域片段),由兩條重鏈組成。根據抗體類型不同,該區域的每一條重鏈由2個或者3個恆定結構域組成。因此,Fc區可通過與特定類型的Fc感受器,或者其它免疫分子如補體蛋白質相結合,來確保每個抗體可對一特定抗原產生一個正確的免疫應答。通過這一過程,可引發不同的生理學效果,包括識別調理顆粒、細胞溶解,以及肥大細胞、嗜鹼性粒細胞和嗜酸性粒細胞的脫顆粒過程。
抗體指機體的免疫系統在抗原刺激下,由B 淋巴細胞或記憶細胞增殖分化成的漿 細胞所產生的、可與相應抗原發生特異性結合的免疫球蛋白。主要分佈在血清中,也分佈於組織液及外分泌液中。
概念
最初有人用電泳證明血清中抗體活性在γ球蛋白部分,故曾把抗體統稱為丙種(γ)球蛋白。後來發現,抗體並不都在γ區;並且位於γ區的球蛋白,也不一定都具有抗體活性。
1964年,世界衛生組織舉行專門會議,將具有抗體活性以及與抗體相關的球蛋白統稱為免疫球蛋白(Ig),如骨髓瘤蛋白,巨球蛋白血症、冷球蛋白血症等患者血清中存在的異常免疫球蛋白以及正常人天然存在的免疫球蛋白亞單位等。因而免疫球蛋白是結構化學的概念,而抗體是生物學功能的概念。可以說,所有抗體都是免疫球蛋白,但並非所有免疫球蛋白都是抗體。
結構
抗體是一種高分子球狀血液蛋白質,重量約為150kDa。由於在部分胺基酸殘基中含有糖鏈,抗體也是一種糖蛋白。能發揮功能的基本單位是一個免疫球蛋白單體。在分泌形態的抗體中包括:二聚體IgA、真骨附類魚的四聚體IgM以及哺乳動物的五聚體IgM。
可發生變化的部分稱為V區(或變化區、可變區),而不變的部分稱為C區(或恆定區)。
免疫球蛋白結構域
抗體的單體是一個Y形的分子,有4條多肽鏈組成。其中包括兩條相同的重鏈,以及兩條相同的輕鏈,之間由雙硫鍵連接在一起[16]。每一條鏈均由稱為免疫球蛋白結構域的多個結構域所組成。每一個結構域大約包含70至110個胺基酸,並根據大小和功能分門別類。例如可變域IgV以及恆定域IgC)[20]。它們的摺疊方式很特別:通過兩次β摺疊將另一條鏈捲入其中形成三明治狀,互相之間通過半胱氨酸和其它帶電荷胺基酸緊密結合。
重鏈
哺乳動物的免疫球蛋白重鏈有5種,分別用希臘字母記為:α、δ、ε、γ以及μ。根據重鏈類型的不同,抗體被分為不同的種型,它們被發現依序分別存在於抗體IgA、IgD、IgE、IgG以及IgM中。不同的重鏈其大小和組成各不相同:α和γ大約有450個胺基酸組成,而μ和ε大約有550個胺基酸組成。
每一條重鏈有兩個區域:恆定區與可變區。同種型的抗體,其恆定區都是一樣的,但不同種型之間該區域是不相同的。例如:γ、α以及δ型重鏈由三個免疫球蛋白結構域串聯而成,並且還有一個用於增加彈性的鉸鏈區;而μ及ε型重鏈則包括四個免疫球蛋白結構域。不同B細胞所生產抗體的重鏈可變區是不同的,但是同一個B細胞及其克隆體所生產的不同種型抗體的可變區則是完全相同的。重鏈的可變區由一個結構域組成,包含大110個胺基酸。
輕鏈
免疫球蛋白輕鏈由大約211至217個胺基酸組成,分為兩個結構域,分別是恆定區和可變區。哺乳動物的輕鏈有兩種,分別命名為λ(lambda)和κ(kappa)。每一個抗體的兩個輕鏈永遠是完全相同的,例如對於哺乳動物而言,同一個抗體要麼是λ型,要麼是κ,不會同時存在。在如軟骨魚綱(鯊魚)及真骨下綱的低級脊椎動物中,還可發現其它類型的輕鏈,如ι(iota)型。
CDRs、Fv、Fab以及Fc結構域
抗體的某些部分具有獨特的功能。比如說Y形的臂區,包含了兩個可以結合抗原的點位,是識別外來物的關鍵所在。該區域被稱為Fab區,即抗原結合區段(fragment, antigen binding)。無論是重鏈還是輕鏈,抗原結合區段均包括一個可變區與一個恆定區,其中可變區的互補位成型於抗體單體胺基酸鏈的末端。可變區又被稱為FV區,是與抗體結合的最關鍵區域,無論是輕鏈還是重鏈都包含該區域。實際上可變區的變化並非隨機或者均勻散布的。更具體的說,這些變化分布在三個可變的β摺疊-轉角上,該區域被稱為互補決定區(Complementarity Determining Region,CDR),也叫做高變區。喬西亞(Chothia)等人,以及後來的諾斯等人對互補決定區的結構進行了歸類。在免疫網路理論*中,每個抗體的互補決定區又被稱為獨特型或者基因型。適應性免疫系統的適應過程,就是依靠有各個獨特型之間的互動來進行調整的。
Y形結構的基座的作用是調節免疫細胞的活動,該區域被稱為Fc區(Fragment crystallizable region,可結晶區域片段),由兩條重鏈組成。根據抗體類型不同,該區域的每一條重鏈由2個或者3個恆定結構域組成。因此,Fc區可通過與特定類型的Fc感受器,或者其它免疫分子如補體蛋白質相結合,來確保每個抗體可對一特定抗原產生一個正確的免疫應答。通過這一過程,可引發不同的生理學效果,包括識別調理顆粒、細胞溶解,以及肥大細胞、嗜鹼性粒細胞和嗜酸性粒細胞的脫顆粒過程。
功能
活化的B細胞可分化成兩種不同用途的細胞:生產可溶性抗體的漿細胞,以及用於記憶已接觸過的抗原的記憶B細胞。後者可在體內存活多年,並使得下次再接觸到同樣抗原時,能夠更迅速的做出相應。
胎兒和新生兒體內的抗體是由母親所提供的,是一種被動免疫。在出生後一年內,新生兒就可自行產生許多不同的抗體。由於抗體可以溶解在血液當中,因此它們是體液免疫系統的一部分。體液循環中的抗體,是由應答某一特定抗原如病毒衣殼片段的B細胞克隆子代所產生的。抗體從下列三個方面為免疫力做出貢獻:通過與病原體結合來避免入侵和破壞自身的細胞;通過刺激巨噬細胞等免疫細胞來包裹並清除病原體;以及通過刺激其它免疫應答過程如補體路徑,來消滅病原體。
哺乳動物分泌形態的IgM抗體有五個免疫球蛋白單元,每一個單元(標為1的部分)有兩個抗原表位結合點Fab區。也就是說,一個IgM抗體可以與10個抗原表位相結合
活化的B細胞可分化成兩種不同用途的細胞:生產可溶性抗體的漿細胞,以及用於記憶已接觸過的抗原的記憶B細胞。後者可在體內存活多年,並使得下次再接觸到同樣抗原時,能夠更迅速的做出相應。
胎兒和新生兒體內的抗體是由母親所提供的,是一種被動免疫。在出生後一年內,新生兒就可自行產生許多不同的抗體。由於抗體可以溶解在血液當中,因此它們是體液免疫系統的一部分。體液循環中的抗體,是由應答某一特定抗原如病毒衣殼片段的B細胞克隆子代所產生的。抗體從下列三個方面為免疫力做出貢獻:通過與病原體結合來避免入侵和破壞自身的細胞;通過刺激巨噬細胞等免疫細胞來包裹並清除病原體;以及通過刺激其它免疫應答過程如補體路徑,來消滅病原體。
哺乳動物分泌形態的IgM抗體有五個免疫球蛋白單元,每一個單元(標為1的部分)有兩個抗原表位結合點Fab區。也就是說,一個IgM抗體可以與10個抗原表位相結合
- 補體的活化
- 效應細胞的活化(調理作用)
- 凝集與沉澱反應
- 中和抗體